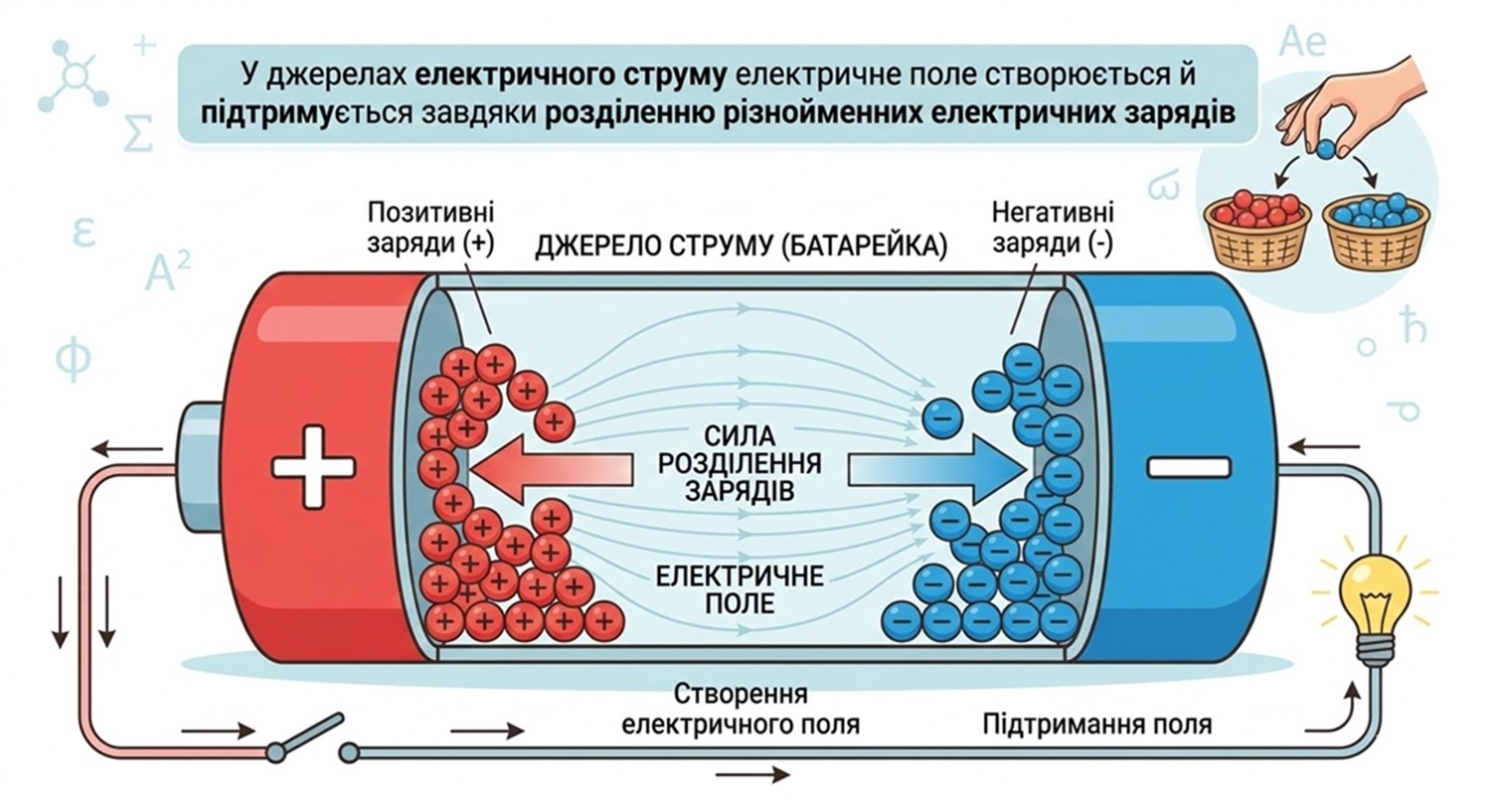

Для подолання сил притягання між різнойменними зарядами та створення електричного поля необхідно виконати роботу. Цей процес відбувається в джерелах струму завдяки перетворенню різних видів енергії (механічної, світлової, хімічної тощо) в електричну.
Джерела електричного струму — пристрої, які перетворюють різні види енергії на електричну енергію.
Усі джерела електричного струму можна умовно розділити на фізичні і хімічні.
До фізичних джерел електричного струму належать пристрої, що перетворюють механічну, світлову або теплову енергію на електричну. У таких механізмах розділення різнойменних зарядів відбувається без участі хімічних реакцій. Прикладами подібних джерел є:

Інтерактивна симуляція "Фізика в школі" (Електрофорна машина)


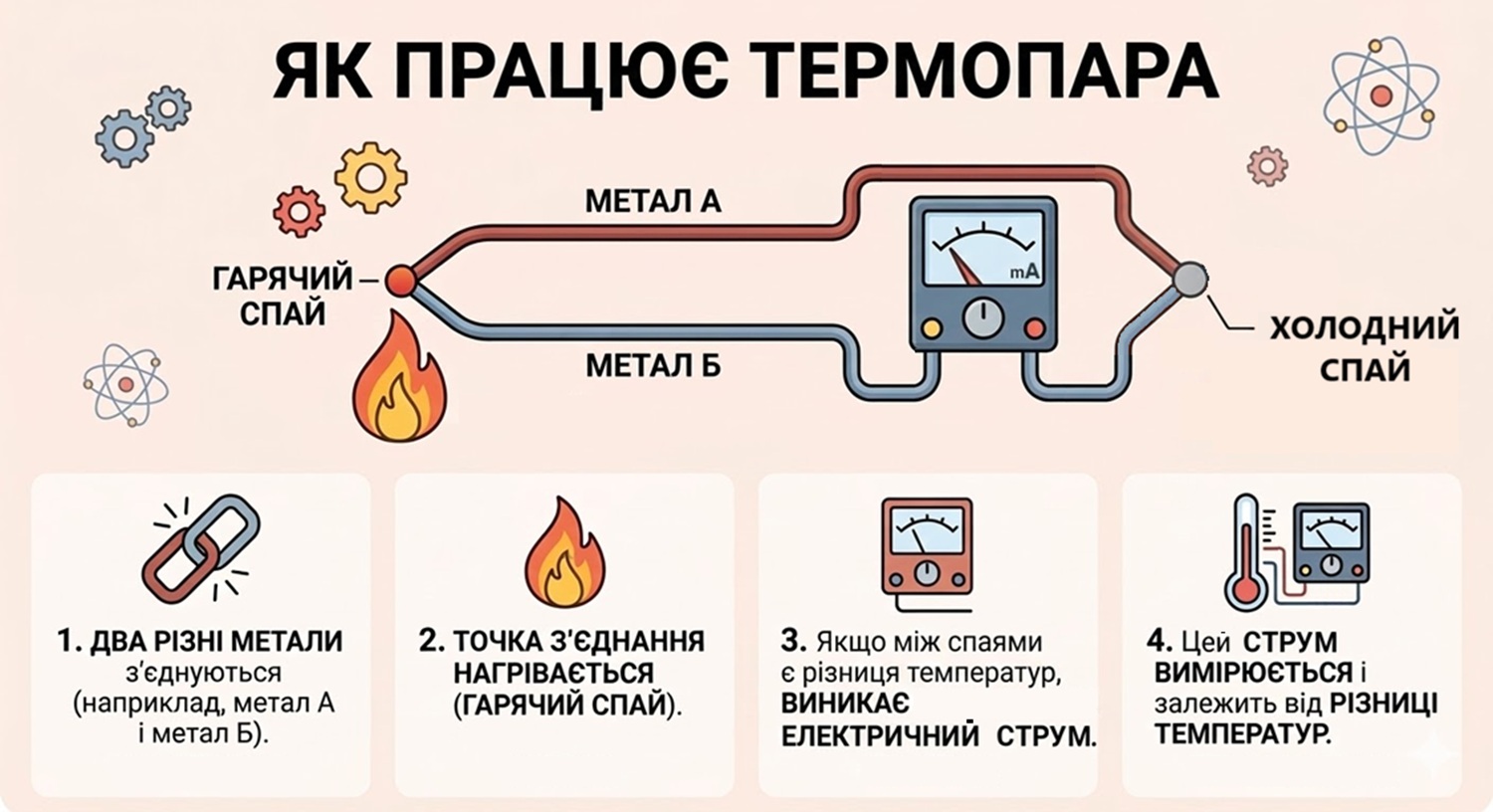
Термопара — пристрій для перетворення теплової енергії на електричну. До кінців константанового дроту (метал А) припаяно два залізні дроти (метал Б), вільні кінці яких з'єднані з гальванометром.
Хімічними джерелами електричного струму називають пристрої, в яких розподіл зарядів відбувається за рахунок енергії, що виділяється внаслідок хімічних реакцій. До хімічних джерел струму належать гальванічні елементи й акумулятори.
Гальванічний елемент створив італійський учений Алессандро Вольта; він назвав його на честь свого співвітчизника — анатома і фізіолога Лу'іджі Ґальвані (1737-1798). Досліди, описані Ґальвані, підказали А. Вольті ідею створення хімічного джерела струму.

Будь-який гальванічний елемент складається з двох електродів та електроліту.
Під час роботи з розчином сульфатної кислоти обов’язково потрібно використовувати захисні окуляри та гумові рукавички, щоб запобігти хімічним опікам шкіри та очей.

Внаслідок хімічної взаємодії металів із електролітом електроди набувають протилежних зарядів: один стає позитивним, а інший — негативним. Робота пристрою триває доти, доки не вичерпається запас активних речовин, після чого хімічні реакції припиняються і струм зникає.
На відміну від гальванічних елементів, які після розряджання стають непридатними, електричні акумулятори можна використовувати повторно. Можливість багаторазового відновлення енергії робить акумулятори особливим видом хімічних джерел струму.
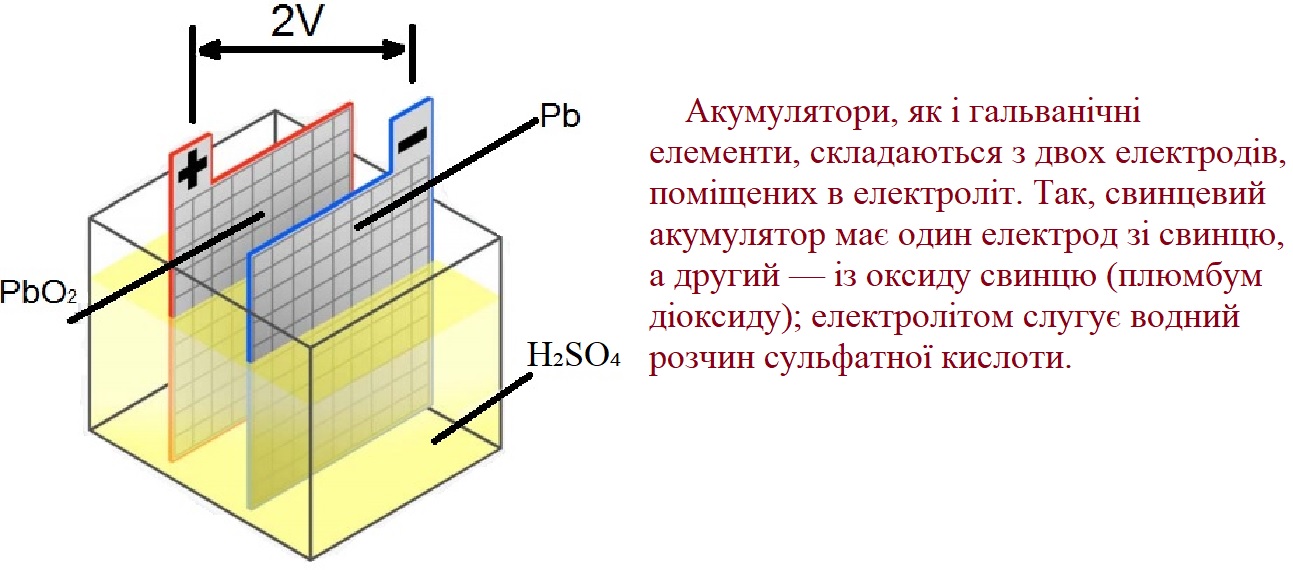
В основі роботи свинцевого акумулятора лежить хімічна взаємодія електродів із розчином сульфатної кислоти, що забезпечує поділ зарядів. Процес розряджання супроводжується зниженням концентрації кислоти, що зрештою призводить до зупинки струму. Завдяки зворотності хімічних процесів, приєднання акумулятора до зовнішнього джерела енергії дозволяє повністю відновити концентрацію електроліту та його працездатність.
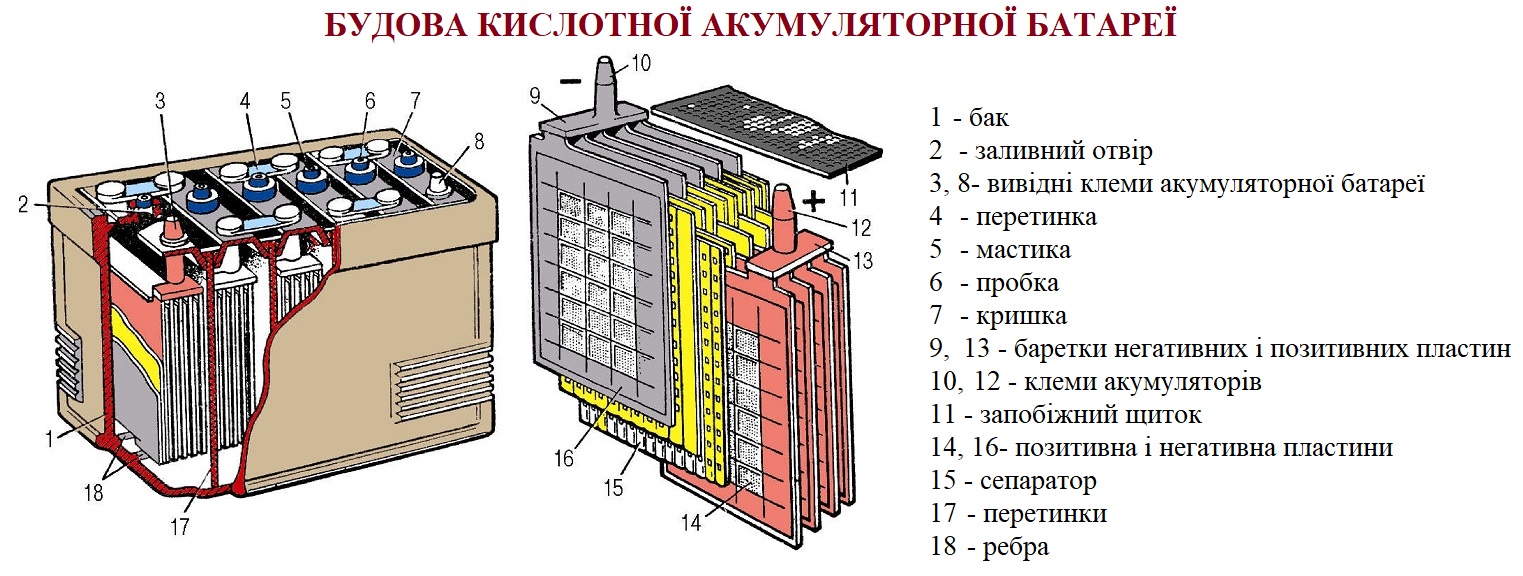
Акумулятори та гальванічні елементи зазвичай об’єднують у батареї, щоб забезпечити необхідну потужність живлення. Таким чином формуються «акумуляторні батареї» та батареї гальванічних елементів, які ми щодня використовуємо в техніці.